|
|
|||||||||||
|
||||||||||||
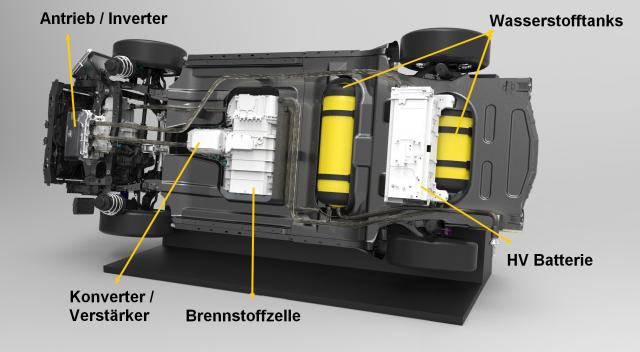
von kfztech.de gehört zur Reihe Elektrotechnische Grundlagen im KfzIn der bishgerigen Reihe über die elektrochemischen Vorgänge im Kfz wurde in Teil 1 die elektrochemische Korrosion behandelt. In Teil 2 wurde die Galvanische Zelle erklärt und in Teil 3 die Starterbatterie besprochen. In Teil 4 soll abschließend auf die Bremstoffzelle eingegangen werden. Eine Brennstoffzelle ist wie bereits erwähnt ebenfalls eine galvanische Zelle. Sie wandelt die chemische Reaktionsenergie eines kontinuierlich zugeführten Brennstoffs (meist Wasserstoff) mit einem Oxidationsmittel (meist Sauerstoff) in elektrische Energie um. Brennstoffzellen können die Energie selbst aber nicht speichern. Das Prinzip der Brennstoffzelle lässt sich am einfachsten mit der chemischen Reaktion 2 H2 + O2 → 2 H2O auf den Punkt bringen. Diese Reaktion zur Gewinnung elektrischer Energie wird auch als „kalte Verbrennung“ bezeichnet. Das Funktionsprinzip der Brennstoffzelle ist schon seit ca. 170 Jahren bekannt, und die Technik wird auch schon seit langem angewendet. Werden doch durch sie beispielsweise Unterseeboote angetrieben oder die Akkus Internationalen Raumstation ISS damit aufgeladen. Brennstoffzellen eignen sich zur Wärme- und Stromerzeugung in Häusern ebenso, wie für den Antrieb von Gabelstaplern, Bussen und Nutzfahrzeugen. Die momentan leistungsfähigste stationäre Brennstoffzelle ist eine Hochtemperatur-Brennstoffzelle im bundesdeutschen Forschungszentrum Jülich. Toyota MiraiNach vielen Prototypen und Versuchsträgern in der Vergangenheit, lief 2015 das erste wasserstoffbetriebene Serienmodell auf Basis des Brennstoffzellenfahrzeugs FCV Concept vom Band: der Toyota Mirai.
Toyota schickte 2015 mit dem Mirai das erste Brennstoffzellenfahrzeug auf die Straße. - Bild: Toyota (abgeändert)
Im Betrieb sind die CO2-neutralen Brennstoffzellenfahrzeuge schadstofffrei. Die Brennstoffzellen-Limousine Mirai benötigt für den Vortrieb ausschließlich Wasserstoff, der in der Brennstoffzelle in elektrische Energie umgewandelt wird und den 113 kW/154 PS starken Elektromotor antreibt. Als Emission entsteht dabei lediglich Wasserdampf. Mit einer Tankfüllung fährt der Toyota Mirai bis zu 500 Kilometer weit, auch der Tankstopp dauert mit etwa drei Minuten nicht länger als bei konventionell angetriebenen Fahrzeugen.
Mittlerweile hat der Mirai schon etliche Feuerproben hinter sich gebracht. - Bild: Toyota Im Betrieb sind die CO2-neutralen Brennstoffzellenfahrzeuge schadstofffrei. Die Brennstoffzellen-Limousine Mirai benötigt für den Vortrieb ausschließlich Wasserstoff, der in der Brennstoffzelle in elektrische Energie umgewandelt wird und den 113 kW/154 PS starken Elektromotor antreibt. Als Emission entsteht dabei lediglich Wasserdampf. Mit einer Tankfüllung fährt der Toyota Mirai bis zu 500 Kilometer weit, auch der Tankstopp dauert mit etwa drei Minuten nicht länger als bei konventionell angetriebenen Fahrzeugen. Die Well-to-Wheel Effizienz soll laut Toyota bei 40% liegen. Ein Benzinmotor liegt da nur bei 19%. Für künftige praxistaugliche Einsätze der Brennstoffzelle als elektrischer Antrieb in serienmäßigen Pkw wird die so genannte Protonenaustausch-Membran-Brennstoffzelle (englisch: Proton Exchange Membrane Fuel Cell) favorisiert und forciert weiterentwickelt. Solche PEMFC-Brennstoffzellen basieren in der Regel auf Wasserstoff als Energieträger und erreichen mittlerweile Wirkungsgrade bis zu 60 %. Vom Aufbau her verfügen diese Brennstoffzellen über Elektroden mit eingefrästen Gaskanalstrukturen aus leitfähigem Kunststoff, der mit Carbon-Nanoröhrchen elektrisch leitend gemacht worden ist. Kernstück der PEMFC ist eine Polymermembran (englisch: proton exchange membrane). Diese PE-Membran lässt zwar für Wasserstoff-Protonen durch, stoppt aber gleichzeitig größere Ionen und wirkt für diese isolierend. Das Oxidationsmittel, der Luftsauerstoff, ist dadurch räumlich vom Reduktionsmittel getrennt.
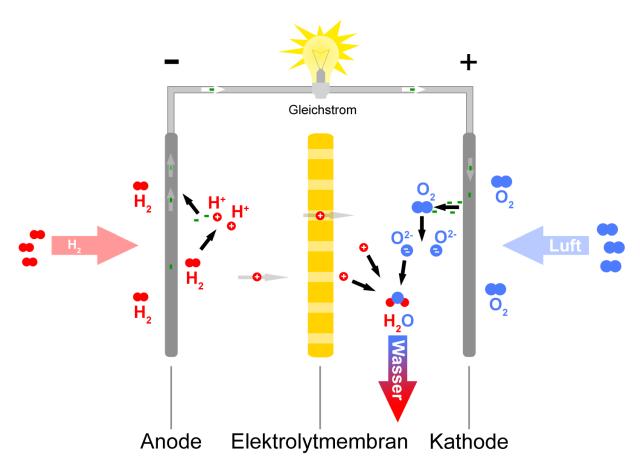
Funktion BrennstoffzelleDie Anode wird mit Wasserstoff als Brennstoff umspült, der dort katalytisch oxidiert und dabei unter Abgabe von Elektronen in Kat-Ionen (H+) umgewandelt wird. Die H+-Ionen gelangen durch die Ionen-Austauschmembran in die Kammer mit dem Oxidationsmittel. Dort werden sie aus der Brennstoffzelle abgeleitet und fließen über einen elektrischen Verbraucher zur Kathode. Die Kathode wird mit Sauerstoff umspült, der durch Aufnahme der Elektronen zu Anionen (O2-) reduziert wird und dann gleichzeitig mit den durch den Elektrolyt zur Kathode gewanderten Protonen zu Wasser (H2O) reagiert.
Funktion der Brennstoffzelle: An der Anode werden Elektronen frei. So wandern die Protonen durch die Membran und reagieren mit den Anionen des Sauerstoffs zu Wasser.- Bild: Wikipedia Public Domain Die so gelieferte Spannung liegt beim derzeitigen Entwicklungsstand zwischen 0,5 und 1,0 Volt. Um eine höhere Spannung zu erhalten, werden mehrere Zellen zu einem Stack (engl. für 'Stapel') in Reihe geschaltet. Einen Video-Link zum Brennstoffzellenauto finden sie hier. Probleme für den dauerhaften Einsatz der Brennstoffzelle im Kfz sind derzeit noch die nur per (afrikanischer) Sonnenenergie CO2-neutrale Gewinnung des Wasserstoffs, die benötigte Tankstellen-Infrastruktur sowie die kompakte Speicherung im Fahrzeug. Außerdem muss die Funktion von Brennstoffzellen auch bei tiefen Minusgraden gewährleistet sein. Zusammenfassung der elektrochemischen Vorgänge im KfzElektrochemische Korrosion beim Automobil erfolgt aufgrund ungewollter chemischer Vorgänge. Davor muss man das Karosserieblech und elektrische Kontakte schützen. Ähnlich laufen auch die Vorgänge in Batterien ab. Dabei handelt es sich prinzipiell um Galvanische Elemente. Man unterscheidet Primärzellen (Batterien), Sekundärzellen (Akkus) und Tertiärzellen (Brennstoffzellen). Fragen für Azubis
Die Antworten findet man im Text der vier Beiträge. Elektrotechnische Grundlagen im Kfz: Kfz-Elektrik | Ladungen | Elektronenbewegung und Leitfähigkeit | el. Strom | Stromwirkungen | Strom messen | Spannung | Spannungserzeugung | Spannung messen | Ohmscher Widerstand |
|
|
|||||||||||
|
||||||||||||